من به تازگی با یک مقاله کلی زیبا با عنوان روبرو شدم اکوسیستم مالی تحقیق و توسعه دارویی. کاغذ سفید برای دولت هلند تهیه شده است و یک نمای کلی از روند توسعه دارو و نحوه (و توسط چه کسی) تامین مالی آن ارائه می دهد. کاغذ سفید به سوالات زیر پاسخ می دهد:
بازیگران مختلف در اکوسیستم توسعه دارو چه می کنند؟
- مؤسسات دانشگاهی و گروههای تحقیقاتی عمومی (PRGs) / سازمانهای غیرانتفاعی 1 اساساً به انتخاب هدف، یعنی شناسایی اهداف بیماریها توجه دارند، اگرچه ممکن است در مراحل بعدی نیز نقش داشته باشند.
- شرکتهای بیوتکنولوژی (بیوتکنولوژی) یا شرکتهای بیودارویی کوچک/متوسط (SMEs) بیشترین فعالیت را در زمینه کشف دارو، توسعه پیش بالینی و توسعه بالینی در مراحل اولیه دارند. کشف دارو شامل یافتن و بهینه سازی یک داروی کاندید است که با هدف بیماری تعامل دارد. در مرحله توسعه پیش بالینی، پروفایلهای ایمنی و کارایی داروی کاندید در مدلهای حیوانی و متعاقباً در آزمایشهای انسانی در مراحل بالینی-توسعه آزمایش میشوند.
- شرکتهای بیودارویی متوسط/بزرگ (بیوفارمای بزرگ) در کل زنجیره ارزش فعال هستند. آنها مجریان توسعه بالینی در مراحل آخر هستند. این مسئولیت معمولاً از پایان فاز 1 یا در طول فاز 2 به بیوفارماهای بزرگ منتقل می شود. با این حال، شرکت های بیوتکنولوژی/SME که به دنبال تجاری سازی دارایی های خود هستند، به طور فزاینده ای چنین کاری را انجام می دهند.
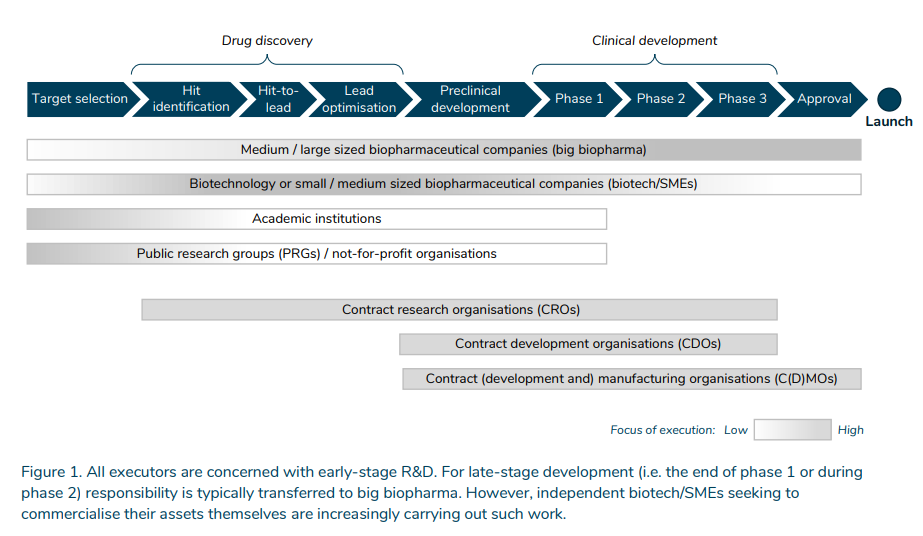
کهن الگوهای معمولی از نحوه تعامل ذینفعان مختلف در فرآیند توسعه دارو چیست؟
این مقاله همچنین 7 کهن الگوی مختلف را برای توسعه دارو فهرست می کند.
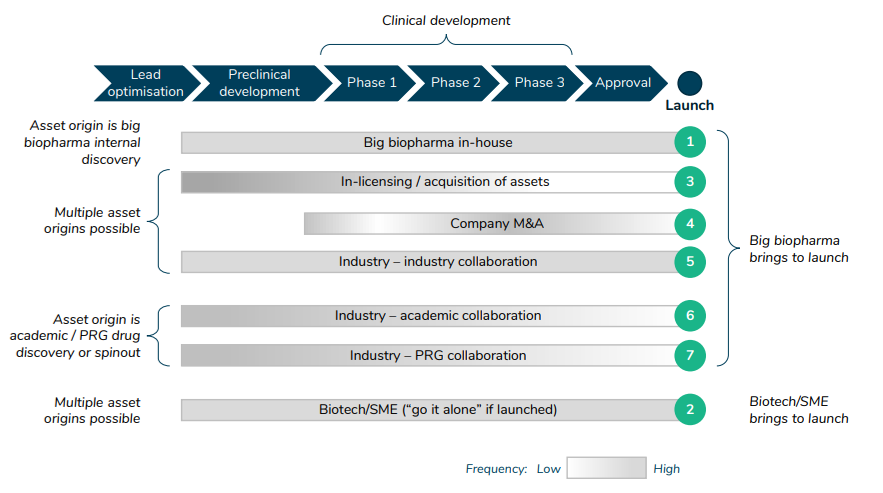
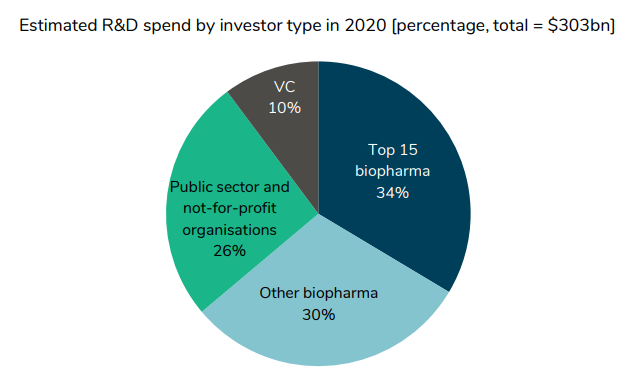
چه کسی توسعه دارو را تامین مالی می کند؟
حدود دو سوم از شرکت های علوم زیستی بخش خصوصی است. با این حال، می بینیم که بین سال های 2011-2019، بودجه بخش خصوصی رشد کرده است. بودجه VC 14.2٪ در سال، biopharma 4.1٪ رشد کرده است، اما بخش عمومی و غیرانتفاعی به ترتیب تنها 1.1٪ و 0.8٪ رشد کرده اند.
یک مطالعه موردی در مورد نحوه تعامل شرکتهای غیرانتفاعی و تأمین مالی بیوداروها با توسعه اخیر داروهای متعدد فیبروز کیستیک نشان داده شده است.
از آنجایی که در اواخر دهه 1990 تنها چند روش درمانی برای درمان علائم فیبروز کیستیک (CF) در دسترس بود، بنیاد سیستیک فیبروزیس (CFF) به دنبال حمایت از توسعه درمانهای اصلاحکننده بیماری بود. CFF میخواست سرمایهگذاری استراتژیک در شرکتهای داروسازی با هدف توسعه درمان سیستیک فیبروزیس انجام دهد. در سال 2000، CFF با Aurora Biosciences برای شناسایی مولکول های اصلاح کننده بیماری همکاری کرد. Vertex Pharma در سال 2001 شرکت Aurora Biosciences را خریداری کرد اما به دلیل تمرکز استراتژیک شدید بر ویروس شناسی، سرمایه گذاری زیادی در این امتیاز CF نکرد. هنگامی که Kalydeco در سال 2006 وارد فاز 1 آزمایشی شد، CFF مبلغ 37 میلیون دلار اضافی را تأمین کرد. نتایج موفقیتآمیز این مرحله ورتکس را تشویق کرد تا در ایجاد قابلیتهای تحقیق و توسعه بیشتر و تجاریسازی برای امتیاز CF سرمایهگذاری کند. علاوه بر این، CFF پس از شروع آزمایشات فاز 2، 75 میلیون دلار اضافی را تأمین مالی کرد. پس از تصویب در سال 2012، Kalydeco از نظر تجاری موفق شد. CFF از فروش حقوق حق امتیاز خود برای Kalydeco در یک معامله 3.3 میلیارد دلاری که در تحقیقات CF مجدداً سرمایه گذاری کرد سود برد.
هزینه تولید دارو چقدر است؟
گرونه:
صرف نظر از راهاندازی موفقیتآمیز یا نه، هزینههای تحقیق و توسعه یک شرکت مجری برای یک ترکیب حدود 280 تا 380 میلیون دلار تخمین زده میشود. با این حال، اگر هزینههای تحقیق و توسعه داروهایی را که شکست میخورند، شامل شود، هزینههای برآورد شده برای سیستم برای توسعه یک داروی تایید شده به طور قابلتوجهی به 1.2 تا 1.7 میلیارد دلار افزایش مییابد (§2.3.2). با اضافه کردن هزینه سرمایه، کل هزینه تحقیق و توسعه سیستم به 2.4 تا 3.2 میلیارد دلار برای هر داروی تایید شده بالغ می شود.
بیش از صرف هزینه، عدم اطمینان است. دولتی، غیرانتفاعی و سرمایه گذاری خطرپذیر به پر کردن «شکاف ترجمه» بین تحقیقات علمی پایه اولیه در انتخاب هدف و کشف دارو و آزمایشهای پیش بالینی و بالینی کمک میکند.
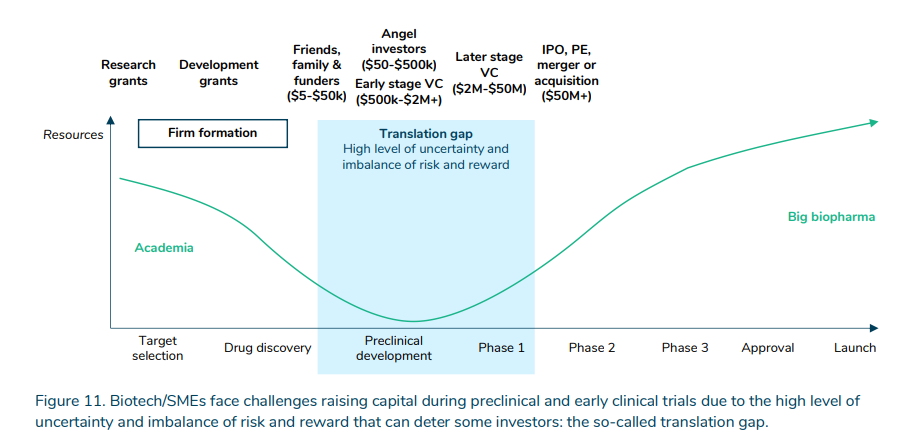
سرمایه گذاری تحقیق و توسعه چقدر به درآمد دارو و/یا اندازه بازار پاسخگو است؟
یک رقم کلیدی این است که چگونه توسعه دارو پاسخگو به درآمد مورد انتظار است. این کشش از 0.3 تا 2.0 > متغیر است، اما شکل زیر بر مطالعات جدیدتر متمرکز است که در آن محدوده 0.3 تا 1.0 است.
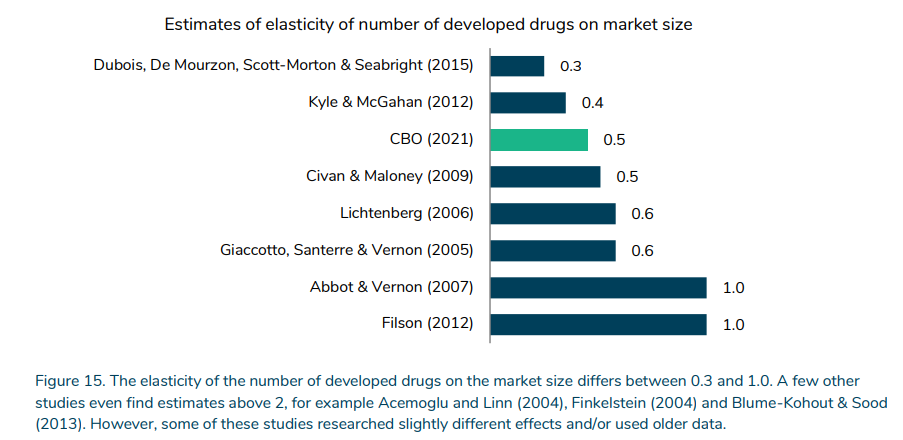
گزارش کامل را می توانید اینجا بخوانید.